السرطان

فهم شامل للمرض، أنواعه، العلاجات المتاحة، وطرق الكشف المبكر
السرطان، كلمة تثير القلق والرهبة في النفوس، هو مجموعة معقدة من الأمراض التي تتسم بالنمو غير المنضبط للخلايا. إنه ليس مرضًا واحدًا، بل مئات الأمراض التي يمكن أن تؤثر على أي جزء من الجسم. في جوهره، ينشأ السرطان عندما تفقد الخلايا الطبيعية آلياتها التنظيمية وتنمو وتتكاثر بشكل لا يمكن السيطرة عليه، مكونة أورامًا يمكن أن تغزو الأنسجة المجاورة وتنتشر إلى أجزاء أخرى من الجسم.
لفهم السرطان بشكل كامل، يجب أن نغوص في بيولوجيا الخلية. أجسامنا تتكون من تريليونات الخلايا التي تنمو، تنقسم، وتموت بطريقة منظمة. هذه العملية محكومة بسلسلة من الإشارات الجينية والبروتينية التي تضمن الحفاظ على توازن دقيق. عندما تحدث طفرات أو تغييرات في الحمض النووي (DNA) داخل الخلايا، يمكن أن تتعطل هذه الإشارات، مما يؤدي إلى نمو خلوي غير طبيعي. هذه الطفرات يمكن أن تكون موروثة، أو يمكن أن تحدث خلال حياة الفرد نتيجة للتعرض لعوامل بيئية مثل المواد الكيميائية المسرطنة، الإشعاع، أو بعض أنواع العدوى الفيروسية والبكتيرية.
تاريخيًا، كان السرطان مرضًا غامضًا ومخيفًا، وغالبًا ما كان يُنظر إليه على أنه حكم بالإعدام. ومع ذلك، بفضل عقود من البحث العلمي المكثف، تطور فهمنا للمرض بشكل كبير. لم نعد ننظر إليه ككيان واحد، بل كطيف واسع من الأمراض التي تتطلب مقاربات علاجية فردية. هذا التقدم أدى إلى تحسينات هائلة في معدلات البقاء على قيد الحياة وجودة حياة المرضى. اليوم، أصبح السرطان في كثير من الحالات مرضًا مزمنًا يمكن إدارته، وفي بعض الحالات، يمكن الشفاء منه تمامًا، خاصة إذا تم اكتشافه في مراحله المبكرة.
تأثير السرطان لا يقتصر على الجانب الجسدي فحسب، بل يمتد ليشمل الجوانب النفسية والاجتماعية والاقتصادية. فالتشخيص بالسرطان يمكن أن يكون مدمرًا عاطفيًا للمرضى وعائلاتهم، ويضع ضغطًا هائلاً على الأنظمة الصحية والاقتصادات الوطنية. ولذلك، فإن مكافحة السرطان تتطلب نهجًا شاملاً يجمع بين البحث العلمي، الوقاية، الكشف المبكر، العلاج المتقدم، والرعاية الداعمة.
يهدف هذا المقال إلى تقديم نظرة عامة وشاملة عن السرطان، مع التركيز على أنواعه المختلفة، آليات تطوره، العلاجات المتاحة حاليًا، وأهمية الكشف المبكر في تحسين النتائج. سنستعرض كيف أحدث التقدم العلمي ثورة في فهمنا للسرطان، وكيف يتم تطوير علاجات جديدة تستهدف الخصائص الفريدة للخلايا السرطانية، وكيف يمكن للأفراد والمجتمعات اتخاذ خطوات لتقليل مخاطر الإصابة بالسرطان.
كيف ينشأ السرطان: من الخلية الطبيعية إلى الورم الخبيث
لفهم السرطان، يجب أن نبدأ بفهم الكيفية التي تنمو بها الخلايا الطبيعية وتتكاثر. في الجسم السليم، تخضع الخلايا لعمليات نمو وانقسام وتحكم دقيقة للغاية. عندما تصبح الخلية قديمة أو تالفة، فإنها تخضع لما يسمى “الموت الخلوي المبرمج” (apoptosis)، وهي آلية طبيعية للتخلص من الخلايا غير المرغوب فيها. هذه الدورة الخلوية المنظمة تضمن الحفاظ على صحة الأنسجة والأعضاء.
ينشأ السرطان عندما يحدث خلل في هذه الدورة الخلوية. هذا الخلل غالبًا ما يكون نتيجة لتراكم الطفرات الجينية (genetic mutations) في الحمض النووي (DNA) للخلية. الحمض النووي هو المادة الوراثية التي تحتوي على التعليمات اللازمة لنمو الخلية ووظيفتها. عندما تتغير هذه التعليمات، يمكن أن تفقد الخلية قدرتها على التحكم في نموها وانقسامها.
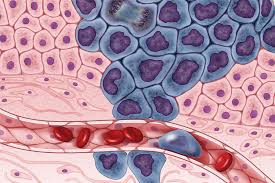
هناك نوعان رئيسيان من الجينات التي تلعب دورًا حاسمًا في تطور السرطان:
- الجينات الورمية البدئية (Proto-oncogenes): هذه الجينات عادة ما تعزز نمو الخلايا الطبيعية وانقسامها. عندما تتحور هذه الجينات وتصبح نشطة بشكل مفرط، فإنها تتحول إلى جينات ورمية (oncogenes). يمكن مقارنة الجينات الورمية البدئية بدواسة البنزين في السيارة؛ عندما تتحول إلى جينات ورمية، فإنها تضغط على دواسة البنزين بشكل مستمر، مما يؤدي إلى تسارع نمو الخلايا.
- الجينات الكابتة للورم (Tumor suppressor genes): هذه الجينات تعمل على إبطاء انقسام الخلايا أو تحفز الموت الخلوي المبرمج، وبالتالي فهي تمنع تكون الأورام. يمكن مقارنتها بالمكابح في السيارة. عندما تحدث طفرات في هذه الجينات، فإنها تفقد وظيفتها، مما يعني أن “المكابح” تفشل، وتستمر الخلايا في النمو دون رادع.
بالإضافة إلى هذه الجينات، تلعب الجينات المسؤولة عن إصلاح الحمض النووي التالف دورًا هامًا أيضًا. إذا كانت هذه الجينات معطوبة، فإن الطفرات يمكن أن تتراكم بسهولة أكبر، مما يزيد من خطر الإصابة بالسرطان.
تطور السرطان هو عملية متعددة الخطوات، تتطلب عادة تراكم العديد من الطفرات الجينية بمرور الوقت. تبدأ الخلية عادة بطفرة واحدة، والتي قد لا تكون كافية لتسبب السرطان في حد ذاتها. ومع ذلك، مع مرور الوقت والتعرض لمزيد من العوامل المسببة للطفرات (المسرطنات)، يمكن أن تتراكم طفرات إضافية، مما يمنح الخلية ميزة نمو غير طبيعية. هذه الخلايا الطافرة تتكاثر، وتشكل مجموعة من الخلايا التي تشارك نفس الطفرات. بمرور الوقت، قد تظهر طفرات جديدة ضمن هذه المجموعة، مما يؤدي إلى ظهور سلالات فرعية من الخلايا السرطانية التي قد تكون أكثر عدوانية أو مقاومة للعلاج.
عوامل الخطر التي تساهم في تطور السرطان
تتفاعل العوامل الوراثية والبيئية ونمط الحياة لتحديد خطر الإصابة بالسرطان. من المهم ملاحظة أن التعرض لعامل خطر لا يعني بالضرورة الإصابة بالسرطان، وأن العديد من الأشخاص الذين يصابون بالسرطان لا يمتلكون أي عوامل خطر معروفة. ومع ذلك، فإن فهم هذه العوامل يساعد في استراتيجيات الوقاية:
- العوامل الوراثية (Genetic Factors): بعض الأشخاص يولدون ولديهم طفرات جينية موروثة تزيد بشكل كبير من خطر إصابتهم بأنواع معينة من السرطان. على سبيل المثال، طفرات في جينات BRCA1 و BRCA2 تزيد من خطر الإصابة بسرطان الثدي والمبيض. ومع ذلك، تشكل السرطانات الوراثية نسبة صغيرة نسبيًا من إجمالي حالات السرطان.
- العوامل البيئية (Environmental Factors):
- التعرض للمواد الكيميائية المسرطنة: مثل دخان التبغ (المسبب الرئيسي لسرطان الرئة، الفم، الحلق، المثانة، وغيرها)، الأسبستوس، البنزين، ومبيدات الآفات.
- التعرض للإشعاع: مثل الأشعة فوق البنفسجية من الشمس (التي تزيد من خطر سرطان الجلد)، والإشعاع المؤين (المستخدم في بعض العلاجات الطبية أو التعرض المهني).
- التلوث: التعرض طويل الأمد لملوثات الهواء يمكن أن يزيد من خطر الإصابة بأنواع معينة من السرطان.
- العوامل المرتبطة بنمط الحياة (Lifestyle Factors):
- التدخين واستهلاك التبغ: يعد السبب الرئيسي للوفيات المرتبطة بالسرطان التي يمكن الوقاية منها.
- السمنة: ترتبط بزيادة خطر الإصابة بالعديد من أنواع السرطان، بما في ذلك سرطان القولون والمستقيم، الثدي (بعد انقطاع الطمث)، بطانة الرحم، والكلى.
- النظام الغذائي غير الصحي: النظام الغذائي الغني باللحوم الحمراء والمعالجة، والفقير في الفواكه والخضروات والألياف، يمكن أن يزيد من خطر الإصابة ببعض أنواع السرطان.
- قلة النشاط البدني: يرتبط بزيادة خطر الإصابة بالعديد من أنواع السرطان، جزئيًا بسبب تأثيره على الوزن والصحة العامة.
- استهلاك الكحول: يزيد من خطر الإصابة بسرطان الفم، الحلق، المريء، الكبد، والثدي.
- العوامل المعدية (Infectious Agents): بعض الفيروسات والبكتيريا يمكن أن تزيد من خطر الإصابة بالسرطان:
- فيروس الورم الحليمي البشري (HPV): المسبب الرئيسي لسرطان عنق الرحم، ويرتبط أيضًا بسرطانات الفم والحلق والشرج.
- التهاب الكبد الفيروسي B و C: يزيدان من خطر الإصابة بسرطان الكبد.
- جرثومة المعدة (Helicobacter pylori): تزيد من خطر الإصابة بسرطان المعدة والأورام اللمفاوية في المعدة.
- فيروس إبشتاين-بار (EBV): يرتبط بأنواع معينة من سرطان الغدد الليمفاوية وسرطان البلعوم الأنفي.
- العمر (Age): السرطان هو في الأساس مرض يصيب التقدم في العمر. كلما تقدمنا في العمر، زاد تراكم الطفرات في خلايانا، وزاد الوقت الذي يمكن أن تتعرض فيه خلايانا للمسرطنات.
تتفاعل هذه العوامل بطرق معقدة، وفي كثير من الحالات، يكون السرطان نتيجة لمجموعة من هذه التأثيرات بدلاً من عامل واحد.
أنواع السرطان: تنوع هائل يتطلب فهمًا دقيقًا
كما ذكرنا، السرطان ليس مرضًا واحدًا، بل هو مصطلح شامل يضم أكثر من 100 نوع مختلف، يتم تصنيفها غالبًا بناءً على نوع الخلية التي نشأت منها أو العضو الذي بدأت فيه. فهم هذا التنوع أمر بالغ الأهمية، حيث أن لكل نوع من أنواع السرطان خصائصه البيولوجية الفريدة، والتي تؤثر على كيفية نموه، انتشاره، واستجابته للعلاج.
يمكن تصنيف السرطانات بشكل عام إلى المجموعات الرئيسية التالية:
- السرطانات (Carcinomas):
- تنشأ هذه السرطانات من الخلايا الظهارية (epithelial cells)، وهي الخلايا التي تغطي الأسطح الداخلية والخارجية للجسم. تشكل هذه الخلايا الجلد، وبطانة الأعضاء الداخلية، والغدد.
- تعتبر السرطانات هي النوع الأكثر شيوعًا، حيث تمثل حوالي 80-90% من جميع حالات السرطان.
- أمثلة: سرطان الرئة، سرطان الثدي، سرطان القولون والمستقيم، سرطان البروستاتا، سرطان البنكرياس، سرطان المبيض، سرطان الجلد (باستثناء الميلانوما).
- يمكن تقسيم السرطانات الفرعية إلى:
- السرطان الغدي (Adenocarcinoma): ينشأ في الخلايا الغدية التي تنتج السوائل والمخاط، مثل سرطان الثدي والقولون والبروستاتا والرئة.
- السرطانة حرشفية الخلايا (Squamous Cell Carcinoma): تنشأ في الخلايا الحرشفية التي تبطن الأعضاء، مثل سرطان الجلد، الرئة، المريء، وعنق الرحم.
- السرطانة الخلايا القاعدية (Basal Cell Carcinoma): النوع الأكثر شيوعًا من سرطان الجلد، وينشأ في الخلايا القاعدية للطبقة الخارجية من الجلد.
- الساركوما (Sarcomas):
- تنشأ الساركوما من الخلايا الموجودة في الأنسجة الرخوة (مثل العضلات، الدهون، الأوعية الدموية، الأعصاب، الأوتار، الأربطة) أو العظام.
- تعتبر أقل شيوعًا بكثير من السرطانات.
- أمثلة: الساركوما العظمية (osteosarcoma) التي تنشأ في العظام، والساركوما الليفية (fibrosarcoma) التي تنشأ في الأنسجة الليفية.
- اللوكيميا (Leukemias):
- هي سرطانات الدم ونخاع العظم (نقي العظم). لا تشكل أورامًا صلبة.
- تنشأ اللوكيميا عندما تنتج خلايا الدم البيضاء غير الناضجة (الأرومات) بكميات كبيرة بشكل غير طبيعي في نخاع العظم، مما يعوق إنتاج خلايا الدم الطبيعية.
- تُصنف اللوكيميا عادةً بناءً على سرعة تطور المرض (حاد أو مزمن) ونوع الخلية المصابة (لمفاوية أو نقوية).
- أمثلة: اللوكيميا الليمفاوية الحادة (ALL)، اللوكيميا النقوية الحادة (AML)، اللوكيميا الليمفاوية المزمنة (CLL)، واللوكيميا النقوية المزمنة (CML).
- الأورام اللمفاوية (Lymphomas):
- هي سرطانات الجهاز الليمفاوي، وهو جزء من الجهاز المناعي. ينشأ من الخلايا الليمفاوية (نوع من خلايا الدم البيضاء) التي توجد في العقد الليمفاوية، الطحال، نخاع العظم، والتوتة.
- تُصنف الأورام اللمفاوية بشكل رئيسي إلى نوعين:
- لمفوما هودجكين (Hodgkin Lymphoma): تتميز بوجود نوع معين من الخلايا السرطانية تسمى خلايا ريد-ستيرنبرغ (Reed-Sternberg cells).
- لمفوما اللاهودجكين (Non-Hodgkin Lymphoma): تشمل مجموعة واسعة من الأورام اللمفاوية التي لا تحتوي على خلايا ريد-ستيرنبرغ.
- الورم النقوي المتعدد (Multiple Myeloma):
- هو سرطان ينشأ في خلايا البلازما (نوع من خلايا الدم البيضاء) الموجودة في نخاع العظم. خلايا البلازما الطبيعية تنتج أجسامًا مضادة لمكافحة العدوى. في الورم النقوي المتعدد، تتراكم خلايا البلازما السرطانية في نخاع العظم وتنتج بروتينات غير طبيعية يمكن أن تلحق الضرر بالكلى والعظام.
- أورام الجهاز العصبي المركزي (Central Nervous System Cancers):
- تشمل الأورام التي تنشأ في الدماغ والحبل الشوكي.
- تسمى هذه الأورام غالبًا بناءً على نوع الخلية التي نشأت منها، مثل الأورام الدبقية (gliomas) التي تنشأ من الخلايا الدبقية الداعمة في الدماغ.
خصائص السرطان التي تجعله خطيرًا
بصرف النظر عن نوعه، تشترك الخلايا السرطانية في عدة خصائص مميزة تجعلها خطيرة:
- النمو غير المنضبط (Uncontrolled Growth): تتكاثر الخلايا السرطانية بسرعة ولا تتوقف عن الانقسام حتى عندما تكون هناك إشارات لإيقاف النمو.
- القدرة على التهرب من الموت الخلوي المبرمج (Evading Apoptosis): لا تخضع الخلايا السرطانية للبرمجة الطبيعية للموت الخلوي، مما يسمح لها بالاستمرار في البكاثر.
- القدرة على غزو الأنسجة المجاورة (Invasion): تتمتع الخلايا السرطانية بالقدرة على اختراق الأنسجة السليمة المحيطة بها وتدميرها. هذا هو الفرق الرئيسي بين الورم الخبيث (السرطاني) والورم الحميد (غير السرطاني)، فالأورام الحميدة لا تغزو الأنسجة المجاورة ولا تنتشر.
- الانتشار (Metastasis): هي العملية التي تنتشر بها الخلايا السرطانية من الموقع الأصلي (الورم الأولي) إلى أجزاء أخرى من الجسم عبر مجرى الدم أو الجهاز الليمفاوي، وتشكل أورامًا ثانوية (نقائل). هذه هي الخاصية الأكثر خطورة للسرطان وهي السبب الرئيسي لمعظم الوفيات المرتبطة بالمرض.
- تكوين أوعية دموية جديدة (Angiogenesis): لكي تنمو الأورام وتنتشر، فإنها تحتاج إلى إمدادات دم كافية. تقوم الخلايا السرطانية بتحفيز نمو أوعية دموية جديدة (عملية تسمى تكون الأوعية) لتغذية الورم.
- التهرب من الاستجابة المناعية (Immune Evasion): تستطيع بعض الخلايا السرطانية تطوير آليات للتهرب من اكتشاف وتدمير الجهاز المناعي للجسم.
فهم هذه الأنواع المختلفة وخصائصها البيولوجية أمر حيوي للبحث والتطوير في مجال علاج السرطان، حيث يوجه العلماء والأطباء نحو تطوير علاجات مستهدفة أكثر فعالية لكل نوع فرعي من السرطان.
الكشف المبكر عن السرطان: مفتاح لتحسين النتائج
يعتبر الكشف المبكر عن السرطان حجر الزاوية في زيادة فرص الشفاء وتحسين النتائج العلاجية بشكل كبير. عندما يتم اكتشاف السرطان في مراحله الأولى، يكون الورم عادةً أصغر حجمًا وأكثر قابلية للعلاج، ولم ينتشر بعد إلى أجزاء أخرى من الجسم (لم يحدث له انتشار أو نقائل). على النقيض من ذلك، عندما يتم تشخيص السرطان في مراحله المتأخرة، يكون العلاج أكثر صعوبة وغالبًا ما يهدف إلى إدارة الأعراض وتحسين جودة الحياة بدلاً من الشفاء التام.
تعتمد استراتيجيات الكشف المبكر على ثلاث ركائز أساسية: الوعي بالأعراض، الفحص المنتظم (Screening)، والتشخيص الدقيق.
1. الوعي بالأعراض والعلامات التحذيرية
من الضروري أن يكون الأفراد على دراية بالعلامات والأعراض الشائعة التي قد تشير إلى وجود السرطان، وأن يستشيروا الطبيب فورًا في حال ظهور أي منها. بعض هذه الأعراض عامة ويمكن أن تكون ناجمة عن حالات غير سرطانية، ولكن المثابرة في الاستشارة الطبية هي المفتاح. تشمل العلامات التحذيرية العامة للسرطان ما يلي:
- تغيرات في عادات التبرز أو التبول: إسهال أو إمساك مستمر، دم في البراز، صعوبة في التبول.
- قرحة لا تلتئم: خاصة في الفم أو على الجلد.
- نزيف أو إفراز غير طبيعي: نزيف مهبلي غير طبيعي، دم في البول، نزيف من المستقيم، سعال مصحوب بدم.
- تكتل أو كتلة في أي مكان بالجسم: خاصة في الثدي، الرقبة، البطن، أو الإبط. أي كتلة جديدة أو متغيرة يجب فحصها.
- عسر الهضم أو صعوبة في البلع: مستمرة وغير مبررة.
- تغير واضح في ثؤلول أو شامة: تغيير في الحجم، الشكل، اللون، أو وجود حكة أو نزيف. (خاصة علامات ABCDE للميلانوما: التناظر Asymmetry، الحواف Borders، اللون Color، القطر Diameter، التطور Evolving).
- سعال أو بحة مستمرة: لا تزول.
- تغيرات في الوزن غير المبررة: فقدان وزن غير مفسر أو زيادة وزن غير مفسرة.
- التعب الشديد والمستمر (Fatigue): لا يتحسن بالراحة.
- التعرق الليلي الشديد والحمى غير المبررة.
الوعي بهذه العلامات لا يعني الهلع، بل يعني أن تكون يقظًا وتطلب المشورة الطبية عند الضرورة.
2. الفحص المنتظم (Cancer Screening)
الفحص المنتظم هو عملية اختبار الأشخاص الأصحاء الذين لا تظهر عليهم أعراض، ولكن لديهم عوامل خطر أو يندرجون ضمن الفئات العمرية المعرضة لخطر الإصابة بنوع معين من السرطان. الهدف هو اكتشاف السرطان قبل ظهور الأعراض، عندما يكون العلاج أكثر فعالية. برامج الفحص الفعالة يمكن أن تقلل بشكل كبير من معدلات الوفيات.
أمثلة على برامج الفحص الشائعة والفعالة:
- فحص سرطان الثدي (Mammography):
- الماموجرام هو أشعة سينية خاصة للثدي تساعد على اكتشاف الأورام أو التغيرات الصغيرة في أنسجة الثدي قبل أن تكون محسوسة.
- يوصى به عادة للنساء فوق سن معينة (عادة 40 أو 50 عامًا، حسب الإرشادات المحلية والتاريخ العائلي)، ويتم إجراؤه بشكل دوري (كل سنة أو سنتين).
- وقد أثبتت فعاليتها في تقليل وفيات سرطان الثدي.
- فحص سرطان عنق الرحم (Cervical Cancer Screening – Pap Test/HPV Test):
- اختبار عنق الرحم (Pap Test): يجمع خلايا من عنق الرحم للبحث عن تغيرات غير طبيعية قد تشير إلى مرحلة ما قبل السرطان أو السرطان المبكر.
- اختبار فيروس الورم الحليمي البشري (HPV Test): يبحث عن وجود فيروس HPV، وهو السبب الرئيسي لسرطان عنق الرحم.
- يوصى به للنساء في سن معينة وبتردد محدد، وغالبًا ما يتم دمج الاختبارين. وقد أدت برامج الفحص هذه إلى انخفاض كبير في معدلات الإصابة والوفيات بسرطان عنق الرحم.
- فحص سرطان القولون والمستقيم (Colorectal Cancer Screening):
- توجد عدة طرق للفحص:
- تنظير القولون (Colonoscopy): هو فحص للكشف عن الأورام الحميدة (الزوائد اللحمية) التي يمكن إزالتها قبل أن تتحول إلى سرطان، أو للكشف عن السرطان في مراحله المبكرة. يوصى به عادةً للأشخاص الذين تبلغ أعمارهم 45-50 عامًا وما فوق، أو في سن مبكرة لمن لديهم تاريخ عائلي.
- اختبار الدم الخفي في البراز (FOBT/FIT): يبحث عن وجود دم في البراز قد يشير إلى وجود زوائد لحمية أو سرطان.
- التنظير السيني المرن (Flexible Sigmoidoscopy): يفحص الجزء السفلي من القولون.
- تساعد هذه الفحوصات في اكتشاف السرطان أو الزوائد اللحمية في مراحل مبكرة، مما يزيد من فرص العلاج الناجح.
- توجد عدة طرق للفحص:
- فحص سرطان الرئة (Lung Cancer Screening):
- يوصى به للمدخنين الحاليين أو السابقين الشرهين (الذين لديهم تاريخ تدخين كبير) باستخدام التصوير المقطعي المحوسب بجرعة منخفضة (LDCT).
- يهدف إلى الكشف عن سرطان الرئة في مراحله المبكرة لدى الأشخاص الأكثر عرضة للخطر.
- فحص سرطان البروستاتا (Prostate Cancer Screening):
- يتضمن عادةً اختبار مستضد البروستاتا النوعي (PSA) وفحص المستقيم الرقمي (DRE).
- الجدل حول فوائد ومخاطر الفحص لهذا النوع من السرطان لا يزال مستمرًا، وغالبًا ما يتم اتخاذ القرار بناءً على مناقشة بين المريض والطبيب حول العوامل الفردية.
من المهم ملاحظة أن التوصيات الخاصة بالفحص تختلف حسب العمر، الجنس، التاريخ العائلي، وعوامل الخطر الأخرى، ويجب مناقشة الخيارات مع الطبيب.
3. التشخيص الدقيق (Accurate Diagnosis)
بمجرد وجود شك في وجود السرطان بناءً على الأعراض أو نتائج الفحص، يتم اتخاذ خطوات للتشخيص الدقيق:
- الفحص السريري والتاريخ الطبي: يقوم الطبيب بفحص المريض وجمع معلومات مفصلة عن الأعراض، التاريخ الطبي الشخصي والعائلي.
- الفحوصات التصويرية: مثل الأشعة السينية (X-rays)، التصوير المقطعي المحوسب (CT scans)، الرنين المغناطيسي (MRI)، التصوير بالموجات فوق الصوتية (Ultrasound)، والتصوير المقطعي بالإصدار البوزيتروني (PET scans). هذه الفحوصات تساعد في تحديد موقع الورم، حجمه، ومدى انتشاره.
- الفحوصات المخبرية: مثل اختبارات الدم والبول، والتي يمكن أن تكشف عن علامات معينة للسرطان (مثل الواسمات الورمية) أو تشوهات في تعداد خلايا الدم.
- الخزعة (Biopsy): هي المعيار الذهبي لتشخيص السرطان. تتضمن أخذ عينة صغيرة من الأنسجة المشتبه بها وفحصها تحت المجهر بواسطة أخصائي علم الأمراض. يمكن للخزعة تأكيد وجود الخلايا السرطانية، تحديد نوع السرطان، ودرجته (مدى عدوانيته).
- الاختبارات الجزيئية والجينومية: تُجرى هذه الاختبارات على عينات الورم لتحديد طفرات جينية محددة أو تغيرات جزيئية، والتي يمكن أن تساعد في توجيه العلاج (خاصة العلاجات الموجهة والعلاجات المناعية).
الجمع بين هذه الأدوات التشخيصية يسمح للأطباء بتشخيص السرطان بدقة، وتحديد مرحلته (Stage) – حجم الورم وما إذا كان قد انتشر – وهو أمر بالغ الأهمية لتخطيط العلاج. الكشف المبكر والتشخيص الدقيق لا ينقذان الأرواح فحسب، بل يقللان أيضًا من العبء الجسدي والنفسي للمرض، ويزيدان من فرص العلاج الأقل عدوانية وذات الآثار الجانبية الأقل.
العلاجات المتاحة للسرطان: ثورة في الرعاية
تطور علاج السرطان بشكل كبير خلال العقود الماضية، وتحول من نهج واحد يناسب الجميع إلى نهج فردي للغاية يعتمد على نوع السرطان، مرحلته، الخصائص الجزيئية للورم، والحالة الصحية العامة للمريض. الهدف من العلاج يمكن أن يكون الشفاء التام، أو إطالة العمر، أو تخفيف الأعراض وتحسين جودة الحياة (الرعاية التلطيفية). غالبًا ما يتم استخدام مجموعة من العلاجات في خطة متعددة التخصصات.
تشمل العلاجات الرئيسية للسرطان ما يلي:
1. الجراحة (Surgery)
تعتبر الجراحة واحدة من أقدم وأكثر طرق علاج السرطان فعالية، خاصة في المراحل المبكرة عندما يكون الورم موضعيًا ولم ينتشر. الهدف الرئيسي للجراحة هو إزالة الورم الخبيث بالكامل، بالإضافة إلى جزء من الأنسجة السليمة المحيطة به لضمان إزالة جميع الخلايا السرطانية. يمكن أيضًا إزالة العقد الليمفاوية القريبة إذا كان هناك اشتباه في انتشار السرطان إليها.
- متى تستخدم؟ تستخدم الجراحة غالبًا لـ:
- إزالة الأورام الصلبة.
- تخفيف الأعراض (جراحة تلطيفية)، مثل إزالة ورم يسبب الألم أو الانسداد.
- أخذ خزعة لتشخيص السرطان.
- إعادة بناء الأنسجة بعد إزالة الورم (مثل جراحة إعادة بناء الثدي بعد استئصاله).
- المزايا: إزالة فورية للورم، خاصة إذا كان موضعيًا.
- العيوب/المخاطر: الألم، العدوى، النزيف، تلف الأعضاء المجاورة، وآثار جانبية طويلة الأمد اعتمادًا على موقع الجراحة (مثل الوذمة اللمفية بعد استئصال العقد الليمفاوية).
2. العلاج الكيميائي (Chemotherapy)
العلاج الكيميائي هو استخدام الأدوية لقتل الخلايا السرطانية أو إبطاء نموها. تعمل هذه الأدوية عادة عن طريق مهاجمة الخلايا سريعة الانقسام، وهو ما يميز الخلايا السرطانية. ومع ذلك، فإنها تؤثر أيضًا على الخلايا الطبيعية سريعة الانقسام في الجسم (مثل خلايا نخاع العظم، بصيلات الشعر، وبطانة الجهاز الهضمي)، مما يسبب العديد من الآثار الجانبية.
- متى تستخدم؟
- العلاج المساعد (Adjuvant Therapy): يُعطى بعد الجراحة لقتل أي خلايا سرطانية متبقية وتقليل خطر تكرار السرطان.
- العلاج المحدِث للتحول (Neoadjuvant Therapy): يُعطى قبل الجراحة أو الإشعاع لتقليص الورم، مما يسهل إزالته أو يجعله أكثر استجابة للعلاج اللاحق.
- العلاج التلطيفي: للتحكم في السرطان المتقدم وتقليل الأعراض.
- علاج السرطانات المنتشرة (المتحولة) أو سرطانات الدم: حيث لا تكون الجراحة خيارًا.
- المزايا: يمكن أن يصل إلى الخلايا السرطانية في جميع أنحاء الجسم.
- العيوب/المخاطر: آثار جانبية واسعة النطاق مثل الغثيان والقيء، تساقط الشعر، التعب، فقر الدم، انخفاض كريات الدم البيضاء (مما يزيد خطر العدوى)، وتلف الأعصاب.
3. العلاج الإشعاعي (Radiation Therapy)
يستخدم العلاج الإشعاعي حزمًا عالية الطاقة (مثل الأشعة السينية أو البروتونات) لقتل الخلايا السرطانية أو إتلاف الحمض النووي الخاص بها، مما يمنعها من النمو والانقسام. يمكن توجيه الإشعاع من خارج الجسم (العلاج الإشعاعي الخارجي) أو عن طريق وضع مصدر مشع داخل الجسم أو بالقرب من الورم (المعالجة الكثبية – Brachytherapy).
- متى تستخدم؟
- علاج رئيسي: لقتل الخلايا السرطانية في ورم موضعي.
- علاج مساعد: بعد الجراحة لقتل الخلايا المتبقية.
- علاج تلطيفي: لتخفيف الألم أو الأعراض الأخرى الناجمة عن الورم.
- يمكن استخدامه بمفرده أو بالاشتراك مع الجراحة والعلاج الكيميائي.
- المزايا: علاج موضعي فعال يمكن أن يدمر الأورام أو يقلصها مع الحفاظ على الأعضاء.
- العيوب/المخاطر: آثار جانبية موضعية تعتمد على المنطقة المعالجة (مثل حروق الجلد، التعب، الغثيان، مشاكل الجهاز الهضمي أو البولي).
4. العلاج الموجه (Targeted Therapy)
العلاجات الموجهة هي فئة جديدة نسبيًا من الأدوية التي تستهدف جزيئات محددة (بروتينات أو جينات) تشارك في نمو الخلايا السرطانية وبقائها. على عكس العلاج الكيميائي الذي يهاجم الخلايا سريعة الانقسام بشكل عام، تستهدف هذه الأدوية الخلايا السرطانية بشكل أكثر تحديدًا، مما يقلل من الضرر الذي يلحق بالخلايا السليمة.
- كيف يعمل؟ يستهدف العلاج الموجه المسارات الخلوية أو الجزيئات التي تكون ضرورية لنمو الورم وانتشاره. على سبيل المثال، قد تستهدف الأدوية المستقبِلات الموجودة على سطح الخلايا السرطانية التي تحفز النمو، أو الإنزيمات داخل الخلايا السرطانية التي تساعدها على البقاء.
- متى تستخدم؟ تستخدم لعلاج أنواع معينة من السرطان التي تحتوي على أهداف جزيئية محددة، مثل بعض أنواع سرطان الثدي (HER2-positive)، سرطان الرئة (EGFR mutations)، وسرطان الجلد (B-RAF mutations). يتطلب ذلك عادةً اختبارات جينية للورم لتحديد ما إذا كان العلاج الموجه مناسبًا.
- المزايا: آثار جانبية أقل حدة بشكل عام من العلاج الكيميائي التقليدي، وفعالية عالية في المرضى الذين لديهم الأهداف الجزيئية المناسبة.
- العيوب/المخاطر: قد يطور السرطان مقاومة للعلاج بمرور الوقت، وقد تكون له آثار جانبية فريدة (مثل مشاكل الجلد، ارتفاع ضغط الدم، مشاكل في القلب).
5. العلاج المناعي (Immunotherapy)
العلاج المناعي هو نهج علاجي يستخدم الجهاز المناعي للمريض لمكافحة السرطان. يعمل على تعزيز قدرة الجهاز المناعي على التعرف على الخلايا السرطانية ومهاجمتها. غالبًا ما تتمكن الخلايا السرطانية من التهرب من اكتشاف الجهاز المناعي، لكن العلاج المناعي يساعد الجهاز المناعي على “رؤية” هذه الخلايا ومهاجمتها.
- كيف يعمل؟ هناك عدة أنواع من العلاج المناعي:
- مثبطات نقاط التفتيش المناعية (Immune Checkpoint Inhibitors): تستهدف البروتينات التي تمنع الجهاز المناعي من مهاجمة الخلايا السرطانية (مثل PD-1, PD-L1, CTLA-4)، مما “يطلق العنان” للجهاز المناعي.
- العلاج بالخلايا التائية المعدلة وراثيًا (CAR T-cell therapy): يتم جمع الخلايا التائية للمريض، وتعديلها وراثيًا في المختبر لتعزيز قدرتها على التعرف على الخلايا السرطانية وقتلها، ثم إعادة حقنها في المريض.
- اللقاحات العلاجية للسرطان: تهدف إلى تدريب الجهاز المناعي على التعرف على بروتينات معينة موجودة في الخلايا السرطانية ومهاجمتها.
- متى تستخدم؟ يستخدم لعلاج مجموعة متزايدة من السرطانات، بما في ذلك الميلانوما، سرطان الرئة، سرطان الكلى، سرطان المثانة، أنواع معينة من سرطان الغدد الليمفاوية، وغيرها.
- المزايا: يمكن أن يؤدي إلى استجابات علاجية طويلة الأمد في بعض المرضى، حتى في حالات السرطان المتقدمة.
- العيوب/المخاطر: يمكن أن يسبب آثارًا جانبية ناتجة عن فرط نشاط الجهاز المناعي الذي يهاجم الأنسجة السليمة (مثل الالتهاب في الأعضاء المختلفة)، وتكون التكلفة عالية جدًا.
6. زراعة الخلايا الجذعية (Stem Cell Transplantation)
تُستخدم زراعة الخلايا الجذعية، والمعروفة أيضًا باسم زراعة نخاع العظم، لعلاج بعض سرطانات الدم مثل اللوكيميا والليمفوما والورم النقوي المتعدد. تتضمن هذه العملية إعطاء جرعات عالية من العلاج الكيميائي أو الإشعاعي لقتل الخلايا السرطانية في نخاع العظم، ثم استبدال الخلايا الجذعية المنتجة للدم بخلايا جذعية سليمة (إما من المريض نفسه أو من متبرع).
- متى تستخدم؟ لعلاج بعض أنواع سرطان الدم ونخاع العظم التي لم تستجب للعلاجات الأخرى أو التي تتطلب جرعات عالية جدًا من العلاج.
- المزايا: يمكن أن يوفر علاجًا شافيًا لبعض المرضى.
- العيوب/المخاطر: إجراء مكثف ومحفوف بالمخاطر، مع آثار جانبية خطيرة محتملة مثل العدوى، داء رفض الطعم المزروع للمضيف (GVHD) في الزراعة من متبرع، وتلف الأعضاء.
7. العلاجات الهرمونية (Hormone Therapy)
تُستخدم العلاجات الهرمونية لعلاج أنواع معينة من السرطان التي تعتمد على الهرمونات للنمو، مثل بعض أنواع سرطان الثدي والبروستاتا. تعمل هذه العلاجات عن طريق منع إنتاج الهرمونات أو منع الهرمونات من الوصول إلى الخلايا السرطانية.
- متى تستخدم؟ لسرطانات الثدي الحساسة للهرمونات (HR-positive) وسرطان البروستاتا.
- المزايا: يمكن أن تكون فعالة في السيطرة على السرطان، خاصة في المراحل المبكرة والمتقدمة.
- العيوب/المخاطر: آثار جانبية شبيهة بأعراض انقطاع الطمث (هبات ساخنة، تعرق ليلي) لدى النساء، وضعف جنسي وفقدان الكثافة العظمية لدى الرجال.
الرعاية الداعمة والتلطيفية
بالإضافة إلى العلاجات الموجهة للسرطان، تعد الرعاية الداعمة (Supportive Care) والرعاية التلطيفية (Palliative Care) جزءًا لا يتجزأ من إدارة السرطان. تهدف هذه الرعاية إلى تخفيف الأعراض والآثار الجانبية للعلاج، وتحسين جودة حياة المريض وعائلته.
- إدارة الألم: غالبًا ما يكون الألم مشكلة رئيسية لمرضى السرطان، ويمكن إدارته بفعالية باستخدام الأدوية، العلاج الطبيعي، أو تقنيات أخرى.
- إدارة الغثيان والقيء: وهي آثار جانبية شائعة للعلاج الكيميائي والعلاج الإشعاعي، ويمكن التحكم فيها بالأدوية المضادة للغثيان.
- إدارة التعب: التعب المرتبط بالسرطان يمكن أن يكون منهكًا، ويتطلب غالبًا إدارة شاملة بما في ذلك التغذية، النشاط البدني المناسب، وإدارة النوم.
- الدعم النفسي: التشخيص بالسرطان وعلاجه يمكن أن يكونا مرهقين نفسيًا. الدعم النفسي، الاستشارة، والانضمام إلى مجموعات الدعم يمكن أن يساعد المرضى وأسرهم على التعامل مع التحديات العاطفية.
- التغذية: يمكن أن تتأثر شهية المريض وقدرته على تناول الطعام. أخصائيي التغذية يمكنهم تقديم المشورة لضمان حصول المريض على التغذية الكافية.
- الرعاية التلطيفية: ليست فقط للمرضى في نهاية العمر، بل هي رعاية متخصصة تهدف إلى تخفيف المعاناة وتحسين جودة الحياة للمرضى الذين يعانون من أمراض خطيرة مثل السرطان، ويمكن تقديمها جنبًا إلى جنب مع العلاج النشط.
أهمية النهج المتعدد التخصصات
في الوقت الحاضر، يتم اتخاذ قرارات علاج السرطان غالبًا من قبل فريق متعدد التخصصات من المتخصصين، بما في ذلك أطباء الأورام (Oncologists)، الجراحون، أطباء الأورام بالإشعاع، أخصائيي علم الأمراض، أخصائيي الأشعة، الممرضات المتخصصات، أخصائيي التغذية، وخبراء الرعاية التلطيفية. يسمح هذا النهج الشامل بتطوير خطة علاجية مخصصة لكل مريض، مع الأخذ في الاعتبار جميع جوانب المرض واحتياجات المريض الفردية.
باختصار، أحدث التقدم في فهم بيولوجيا السرطان ثورة في خيارات العلاج، مما أدى إلى علاجات أكثر فعالية وأقل سمية. ومع استمرار البحث، يزداد الأمل في إيجاد علاجات أكثر تقدمًا وشافية في المستقبل.
الوقاية من السرطان: خطوات لتقليل المخاطر
على الرغم من التقدم الكبير في علاج السرطان، تبقى الوقاية هي الاستراتيجية الأكثر فعالية للحد من العبء العالمي للمرض. تشير التقديرات إلى أن نسبة كبيرة من حالات السرطان يمكن الوقاية منها من خلال تبني أنماط حياة صحية وتجنب التعرض لعوامل الخطر المعروفة. تتركز استراتيجيات الوقاية من السرطان على محورين رئيسيين: الوقاية الأولية التي تهدف إلى منع حدوث السرطان في المقام الأول، والوقاية الثانوية التي تركز على الكشف المبكر والتدخل.
1. الوقاية الأولية: تجنب عوامل الخطر وتعديل نمط الحياة
تهدف الوقاية الأولية إلى تقليل التعرض للمسرطنات والعوامل التي تزيد من خطر الإصابة بالسرطان. وتشمل هذه الاستراتيجيات:
- الإقلاع عن التدخين وتجنب التعرض للتبغ:
- يُعد التدخين السبب الرئيسي للوفيات المرتبطة بالسرطان التي يمكن الوقاية منها. يرتبط التدخين بأكثر من 15 نوعًا من السرطانات، بما في ذلك الرئة، الحلق، الفم، المريء، المثانة، البنكرياس، الكلى، وعنق الرحم.
- تجنب التدخين السلبي (التعرض لدخان التبغ من الآخرين) لا يقل أهمية، حيث يزيد أيضًا من خطر الإصابة بالسرطان.
- إن الإقلاع عن التدخين في أي عمر يمكن أن يقلل بشكل كبير من خطر الإصابة بالسرطان.
- الحفاظ على وزن صحي (الوقاية من السمنة):
- السمنة ليست مجرد مشكلة تجميلية؛ إنها عامل خطر رئيسي لأكثر من 13 نوعًا من السرطانات، بما في ذلك سرطان القولون والمستقيم، الثدي (بعد انقطاع الطمث)، بطانة الرحم، الكلى، المريء، البنكرياس، والكبد.
- يرتبط الحفاظ على وزن صحي من خلال نظام غذائي متوازن وممارسة النشاط البدني المنتظم بتقليل خطر الإصابة بهذه السرطانات.
- اتباع نظام غذائي صحي ومتوازن:
- الإكثار من الفواكه والخضروات والحبوب الكاملة: غنية بالألياف، الفيتامينات، المعادن، ومضادات الأكسدة التي قد تحمي الخلايا من التلف.
- الحد من اللحوم الحمراء والمعالجة: تظهر الدراسات أن الاستهلاك المفرط للحوم الحمراء (مثل لحم البقر والضأن) واللحوم المصنعة (مثل النقانق واللحوم الباردة) يزيد من خطر الإصابة بسرطان القولون والمستقيم وأنواع أخرى من السرطان.
- الحد من الأطعمة المصنعة والسكريات المضافة: قد تساهم في السمنة والالتهاب المزمن، وكلاهما يرتبط بزيادة خطر الإصابة بالسرطان.
- تقليل تناول الكحول: يرتبط استهلاك الكحول بزيادة خطر الإصابة بسرطان الفم، الحلق، المريء، الكبد، والثدي. كلما قل استهلاك الكحول، قل الخطر.
- ممارسة النشاط البدني بانتظام:
- النشاط البدني المنتظم (مثل المشي السريع، الركض، السباحة، ركوب الدراجات) لمدة 30 دقيقة على الأقل في معظم أيام الأسبوع يمكن أن يقلل من خطر الإصابة بأنواع عديدة من السرطان، جزئيًا عن طريق المساعدة في الحفاظ على وزن صحي، وتحسين وظيفة الجهاز المناعي، وتقليل الالتهاب.
- الحماية من أشعة الشمس:
- التعرض المفرط للأشعة فوق البنفسجية (UV) من الشمس أو أسرة التسمير هو السبب الرئيسي لسرطان الجلد، بما في ذلك الميلانوما (الشكل الأكثر خطورة).
- يجب استخدام واقي الشمس، ارتداء الملابس الواقية، البحث عن الظل، وتجنب التعرض للشمس في ساعات الذروة (بين 10 صباحًا و 4 مساءً).
- التطعيمات (اللقاحات):
- بعض أنواع السرطان تسببها الفيروسات التي يمكن الوقاية منها باللقاحات.
- لقاح فيروس الورم الحليمي البشري (HPV): يحمي من سلالات فيروس HPV التي تسبب معظم حالات سرطان عنق الرحم، ويرتبط أيضًا بسرطانات أخرى مثل سرطان الشرج، الفم، والحلق. يوصى به للمراهقين (الذكور والإناث) قبل التعرض للفيروس.
- لقاح التهاب الكبد الفيروسي B (HBV): يقلل بشكل كبير من خطر الإصابة بسرطان الكبد المرتبط بالتهاب الكبد المزمن B.
- تجنب التعرض للمواد الكيميائية المسرطنة:
- في بعض المهن، قد يتعرض الأفراد لمواد كيميائية معروفة بأنها مسرطنة (مثل الأسبستوس، البنزين، الديوكسينات). يجب اتخاذ تدابير السلامة المهنية الصارمة لتقليل التعرض.
- تجنب التعرض للملوثات البيئية قدر الإمكان.
2. الوقاية الثانوية: الكشف المبكر والتدخل
تركز الوقاية الثانوية على اكتشاف السرطان في مراحله المبكرة، عندما يكون العلاج أكثر فعالية. وقد ناقشنا هذا بالتفصيل في قسم “الكشف المبكر عن السرطان”. ولكن للتذكير:
- برامج الفحص المنتظم (Screening Programs): مثل الماموجرام لسرطان الثدي، اختبار عنق الرحم (Pap test) وسرطان القولون والمستقيم (تنظير القولون). هذه الفحوصات تكتشف السرطان أو التغيرات ما قبل السرطانية قبل ظهور الأعراض.
- الوعي الذاتي والفحص الذاتي: مثل الفحص الذاتي للثدي، والفحص المنتظم للجلد للكشف عن أي تغيرات في الشامات أو الثآليل.
- التعرف على العلامات التحذيرية واستشارة الطبيب: كما ذكرنا سابقًا، أي أعراض غير مبررة أو مستمرة يجب أن يتم تقييمها من قبل أخصائي الرعاية الصحية.
نمط الحياة الصحي كاستراتيجية وقائية شاملة
يُظهر العلم أن اعتماد نمط حياة صحي شامل هو أحد أقوى الأدوات في مكافحة السرطان. لا يقلل هذا النمط من خطر الإصابة بالسرطان فحسب، بل يساهم أيضًا في الوقاية من العديد من الأمراض المزمنة الأخرى مثل أمراض القلب والسكري. إنه استثمار في الصحة على المدى الطويل.
من المهم تذكر أن الوقاية لا تضمن عدم الإصابة بالسرطان أبدًا، حيث توجد عوامل لا يمكن التحكم فيها مثل الاستعداد الوراثي والطفرات العشوائية. ومع ذلك، فإن تبني هذه الاستراتيجيات الوقائية يزيد بشكل كبير من فرص البقاء بصحة جيدة ويقلل من المخاطر الكلية. إن الجهود المشتركة على المستويات الفردية والمجتمعية والحكومية ضرورية لتعزيز الوعي، وتوفير الموارد، وتطبيق السياسات التي تدعم أنماط الحياة الصحية وتشجع على الفحص المبكر.
مستقبل علاج السرطان والآفاق الواعدة
يعد مجال أبحاث السرطان أحد أكثر المجالات ديناميكية وسرعة في التطور في العلوم الطبية. مع كل يوم يمر، تظهر اكتشافات جديدة تزيد من فهمنا للمرض وتفتح آفاقًا واعدة لعلاجات أكثر فعالية وأقل سمية. يستند هذا التقدم إلى تطورات مذهلة في التكنولوجيا، مثل تسلسل الحمض النووي عالي الإنتاجية، المعلوماتية الحيوية، والذكاء الاصطناعي، مما يمكن العلماء من الغوص في أعماق البيولوجيا الجزيئية للسرطان.
تتركز الجهود البحثية المستقبلية على عدة مجالات رئيسية:
1. الطب الدقيق (Precision Medicine)
يمثل الطب الدقيق مستقبل علاج السرطان. الهدف هو تخصيص العلاج لكل مريض بناءً على الخصائص الجينية والجزيئية الفريدة لورمه. بدلاً من اتباع نهج “مقاس واحد يناسب الجميع”، يتم الآن تحليل الحمض النووي للورم لكل مريض لتحديد الطفرات الجينية المحددة التي تدفع نمو السرطان.
- الاختبارات الجينومية المتقدمة: تسمح هذه الاختبارات بتحديد الطفرات في جينات معينة (مثل EGFR, ALK, BRAF, KRAS) أو التغيرات الجينية الأخرى التي يمكن استهدافها بأدوية معينة.
- تطوير أدوية موجهة جديدة: مع تحديد المزيد من الأهداف الجزيئية، يقوم الباحثون بتطوير أدوية جديدة تستهدف هذه المسارات بشكل دقيق، مما يزيد من الفعالية ويقلل من الآثار الجانبية.
- السوائل الحيوية (Liquid Biopsies): تقنية جديدة واعدة تتضمن تحليل عينة دم للبحث عن الحمض النووي للورم المتداول (ctDNA) أو الخلايا السرطانية المتداولة (CTCs). يمكن استخدامها للكشف عن السرطان مبكرًا، مراقبة الاستجابة للعلاج، واكتشاف المقاومة للأدوية دون الحاجة إلى خزعة جراحية.
2. التوسع في العلاج المناعي
لقد أحدث العلاج المناعي ثورة في علاج العديد من أنواع السرطان، وسيستمر البحث في هذا المجال في التوسع:
- تحديد المزيد من نقاط التفتيش المناعية: البحث مستمر لتحديد بروتينات إضافية يمكن استهدافها لـ “إطلاق العنان” للجهاز المناعي لمكافحة السرطان.
- العلاج المناعي المركب: تُظهر الدراسات أن الجمع بين أنواع مختلفة من العلاج المناعي (أو العلاج المناعي مع علاجات أخرى مثل العلاج الكيميائي أو الإشعاعي) يمكن أن يزيد من معدلات الاستجابة ويطيل البقاء على قيد الحياة.
- العلاج بالخلايا التائية المعدلة (CAR T-cell therapy) للسرطانات الصلبة: على الرغم من نجاحها الكبير في سرطانات الدم، لا تزال فعالية علاج CAR T-cell محدودة في الأورام الصلبة. تُبذل جهود كبيرة لتطوير هذا العلاج ليصبح أكثر فعالية في هذه السرطانات.
- اللقاحات العلاجية المخصصة (Personalized Cancer Vaccines): تطوير لقاحات مصممة خصيصًا لكل مريض، تستهدف البروتينات الفريدة (neoantigens) الموجودة على خلاياه السرطانية، لتدريب الجهاز المناعي على مهاجمة هذه الخلايا بشكل أكثر تحديدًا.
3. تقنيات العلاج الإشعاعي والجراحي المتقدمة
تستمر التطورات في التكنولوجيا في تحسين دقة وفعالية العلاج الإشعاعي والجراحة:
- العلاج بالبروتونات (Proton Therapy): شكل أكثر دقة من العلاج الإشعاعي يمكن أن يقلل من الضرر الذي يلحق بالأنسجة السليمة المحيطة بالورم.
- الجراحة الروبوتية: تتيح إجراء عمليات جراحية أكثر دقة وأقل توغلاً، مما يقلل من مضاعفات ما بعد الجراحة ووقت التعافي.
- تقنيات التصوير الموجهة للجراحة: استخدام تقنيات التصوير المتقدمة أثناء الجراحة لمساعدة الجراحين على رؤية الورم بشكل أفضل وضمان إزالته بالكامل.
4. الوقاية من السرطان وفهم بيولوجيا الورم
لا يزال البحث عن طرق جديدة للوقاية من السرطان أمرًا حيويًا:
- علم الأوبئة الجزيئية: فهم كيف تؤثر العوامل البيئية ونمط الحياة على الجينات والخلايا على المستوى الجزيئي لزيادة خطر الإصابة بالسرطان.
- الوقاية الكيميائية (Chemoprevention): استخدام الأدوية أو المركبات الطبيعية لتقليل خطر الإصابة بالسرطان لدى الأشخاص المعرضين لخطر كبير (على سبيل المثال، بعض الأدوية لتقليل خطر سرطان الثدي).
- فهم ميكروبيوم السرطان: دراسة كيف يمكن للبكتيريا والفيروسات والكائنات الدقيقة الأخرى الموجودة داخل وحول الأورام أن تؤثر على تطور السرطان واستجابته للعلاج.
5. الذكاء الاصطناعي (AI) والتعلم الآلي (Machine Learning) في أبحاث السرطان
يُحدث الذكاء الاصطناعي ثورة في جميع جوانب رعاية السرطان:
- التشخيص المبكر والتصوير: يمكن للذكاء الاصطناعي تحليل صور التصوير الطبي (مثل الماموجرام، الأشعة المقطعية) بدقة أكبر وسرعة للكشف عن الأورام الصغيرة التي قد يغفلها البشر.
- تطوير الأدوية: تسريع عملية اكتشاف الأدوية من خلال تحليل كميات هائلة من البيانات لتحديد الجزيئات الواعدة.
- الطب الدقيق: مساعدة الأطباء على اتخاذ قرارات علاجية مخصصة من خلال تحليل بيانات المريض الشاملة (الجينية، السريرية، نمط الحياة) والتنبؤ بالاستجابة للعلاج.
- اكتشاف الواسمات الحيوية: تحديد علامات جديدة في الدم أو الأنسجة يمكن أن تشير إلى وجود السرطان أو الاستجابة للعلاج.
6. التركيز على جودة الحياة والرعاية التلطيفية
بينما يركز البحث على الشفاء، هناك أيضًا اعتراف متزايد بأهمية تحسين جودة حياة مرضى السرطان ونجاتهم:
- تطوير علاجات ذات آثار جانبية أقل: الأدوية والتكتيكات العلاجية الجديدة التي تقلل من الضرر الذي يلحق بالخلايا السليمة.
- الرعاية التلطيفية المبكرة: دمج الرعاية التلطيفية في وقت مبكر من مسار المرض لتحسين إدارة الأعراض والدعم النفسي.
- البقاء على قيد الحياة بعد السرطان (Survivorship): فهم وإدارة الآثار الجانبية طويلة الأجل للعلاج والتحديات النفسية والاجتماعية التي يواجهها الناجون من السرطان.
مستقبل علاج السرطان مشرق بفضل الابتكارات المستمرة في البحث والتكنولوجيا. على الرغم من أن الطريق لا يزال طويلًا للقضاء على السرطان تمامًا، إلا أن هذه التطورات تمنحنا الأمل في أن نتمكن يومًا ما من تحويل السرطان إلى مرض يمكن علاجه أو الوقاية منه بشكل فعال في جميع الحالات. يستمر التعاون الدولي والاستثمار في البحث العلمي في دفع حدود المعرفة وتوفير حلول جديدة للمرضى في جميع أنحاء العالم.
الخلاصة
السرطان هو تحد صحي عالمي ضخم، ولكنه ليس قوة لا يمكن قهرها. على مدى العقود الماضية، تطور فهمنا لهذا المرض المعقد بشكل كبير، مما أدى إلى تحسينات ملحوظة في التشخيص والعلاج والوقاية. لم يعد السرطان حكمًا نهائيًا في كثير من الحالات، بل أصبح مرضًا يمكن إدارته، وفي أحيان كثيرة، يمكن الشفاء منه، خاصةً عندما يتم اكتشافه في مراحله المبكرة.
لقد استعرضنا في هذا المقال الجوانب المتعددة للسرطان، بدءًا من بيولوجيته الأساسية وكيف ينشأ من خلل في نمو الخلايا، مرورًا بأنواعه المتعددة التي تختلف في خصائصها وسلوكها. رأينا كيف أن الكشف المبكر، سواء من خلال الوعي بالأعراض أو برامج الفحص المنتظمة، يلعب دورًا حاسمًا في زيادة فرص النجاح العلاجي.
كما سلطنا الضوء على مجموعة واسعة من العلاجات المتاحة اليوم، بدءًا من الجراحة والعلاج الكيميائي والإشعاعي التقليدية، وصولًا إلى الابتكارات الثورية مثل العلاجات الموجهة والعلاج المناعي التي تستهدف الخلايا السرطانية بدقة أكبر أو تعزز قدرة الجهاز المناعي على مكافحة المرض. وأكدنا على أهمية الرعاية الداعمة والتلطيفية لضمان أفضل جودة حياة للمرضى.
الأهم من ذلك، تناولنا الدور المحوري للوقاية من السرطان. فمن خلال تبني أنماط حياة صحية – بما في ذلك الإقلاع عن التدخين، الحفاظ على وزن صحي، اتباع نظام غذائي متوازن، وممارسة النشاط البدني – يمكننا تقليل خطر الإصابة بالسرطان بشكل كبير. كما أن التطعيمات ضد بعض الفيروسات المسببة للسرطان، وتجنب التعرض للمسرطنات البيئية، تعد خطوات وقائية حاسمة.
مستقبل مكافحة السرطان يبدو واعدًا. مع التقدم المستمر في الطب الدقيق، والتوسع في العلاج المناعي، وتطوير تقنيات تشخيصية وعلاجية أكثر تطورًا، بالإضافة إلى الاستخدام المتزايد للذكاء الاصطناعي، نحن أقرب من أي وقت مضى إلى تحقيق اختراقات كبيرة. يواصل العلماء والأطباء في جميع أنحاء العالم العمل بلا كلل لفك رموز أسرار السرطان وتطوير استراتيجيات أكثر فعالية للقضاء عليه.
إن مكافحة السرطان تتطلب جهدًا جماعيًا. تبدأ بالوعي الفردي والخيارات الصحية، وتمتد إلى مبادرات الصحة العامة الشاملة، والاستثمار في البحث العلمي، والدعم المستمر للمرضى وعائلاتهم. من خلال العمل معًا، يمكننا أن نرى يومًا يصبح فيه السرطان مجرد ذكرى تاريخية، أو على الأقل، مرضًا يمكن السيطرة عليه بالكامل.