العلاجات الجينية وتحرير الجينات
العلاجات الجينية وتحرير الجينات – آمال وتحديات
شهدت العقود الأخيرة تطورات علمية مذهلة في فهمنا للأساس الجيني للحياة والأمراض. وقد فتحت هذه الاكتشافات آفاقًا جديدة لعلاج الأمراض التي كانت تعتبر في السابق مستعصية، وذلك من خلال التدخل المباشر في المادة الوراثية للإنسان. يمثل العلاج الجيني وتحرير الجينات طليعة هذه الثورة الطبية، حيث يقدمان وعودًا هائلة بالقضاء على الأمراض الوراثية، وعلاج السرطان، وحتى الوقاية من بعض الأمراض المعدية. ومع ذلك، فإن هذه التقنيات تحمل في طياتها تحديات أخلاقية واجتماعية وقانونية يجب معالجتها بعناية لضمان استخدامها بشكل مسؤول وآمن.
1. فهم الأساس: الجينات والأمراض الوراثية
تعتبر الجينات الوحدات الأساسية للوراثة، وهي تتكون من الحمض النووي الريبوزي منقوص الأكسجين (DNA). تحمل هذه الجينات التعليمات اللازمة لبناء وتشغيل الجسم. تتواجد الجينات على شكل أزواج داخل الكروموسومات في نواة كل خلية. يمكن أن تؤدي التغيرات أو الطفرات في تسلسل الحمض النووي داخل الجين إلى تعطيل وظيفته الطبيعية، مما قد يؤدي إلى الإصابة بالأمراض الوراثية.
هناك الآلاف من الأمراض الوراثية المعروفة، والتي تتراوح في شدتها من حالات بسيطة إلى أمراض تهدد الحياة. بعض هذه الأمراض ناتج عن طفرة في جين واحد (مثل التليف الكيسي وفقر الدم المنجلي)، بينما ينتج البعض الآخر عن تفاعلات معقدة بين عدة جينات وعوامل بيئية (مثل بعض أنواع السرطان وأمراض القلب).
2. العلاج الجيني: استبدال وتعديل الجينات المعيبة
يهدف العلاج الجيني إلى علاج أو الوقاية من الأمراض عن طريق إدخال مادة وراثية إلى خلايا المريض أو تعديلها أو استبدالها. يمكن أن تتضمن هذه المادة الوراثية جينًا سليمًا لتعويض جين معيب، أو جينًا جديدًا له تأثير علاجي، أو حتى مادة وراثية تعمل على إسكات جين مسبب للمرض.
2.1 آليات العلاج الجيني:
- إضافة الجينات: يتم إدخال نسخة سليمة من الجين المعيب إلى خلايا المريض. لا يحل هذا الجين الجديد محل الجين المعيب، ولكنه يسمح للخلايا بإنتاج البروتين الضروري الذي كان مفقودًا أو معيبًا.
- استبدال الجينات: يتم استبدال الجين المعيب بنسخة سليمة. هذه الطريقة أكثر تعقيدًا من إضافة الجينات وتتطلب تقنيات دقيقة لتحرير الجينوم.
- إسكات الجينات: يتم استخدام تقنيات مختلفة لتعطيل أو إسكات الجينات التي تسبب المرض. يمكن تحقيق ذلك باستخدام جزيئات صغيرة من الحمض النووي الريبوزي (RNA) تتداخل مع عملية ترجمة الجين إلى بروتين.
- تعديل الجينات: يتم إجراء تغييرات محددة على الجين المعيب لتصحيح الطفرة واستعادة وظيفته الطبيعية.
2.2 طرق توصيل الجينات:
لإيصال المادة الوراثية إلى خلايا المريض، يتم استخدام ما يعرف بـ “النواقل”. هناك نوعان رئيسيان من النواقل:
- النواقل الفيروسية: تستخدم الفيروسات المعدلة وراثيًا كحامل لإيصال الجينات إلى الخلايا. تمتاز الفيروسات بقدرتها الطبيعية على إصابة الخلايا وإدخال مادتها الوراثية إليها. يتم تعديل الفيروسات المستخدمة في العلاج الجيني لجعلها غير قادرة على التكاثر أو إحداث المرض. تشمل أنواع النواقل الفيروسية الشائعة الفيروسات الغدانية (Adenoviruses)، والفيروسات المرتبطة بالغدة (Adeno-associated viruses – AAV)، والفيروسات البطيئة (Lentiviruses).
- النواقل غير الفيروسية: تشمل طرقًا أخرى لإيصال الجينات مثل استخدام البلازميدات (جزيئات دائرية من الحمض النووي)، والليبوسومات (جسيمات دهنية صغيرة)، والجسيمات النانوية. هذه الطرق تعتبر أقل فعالية في توصيل الجينات مقارنة بالنواقل الفيروسية، ولكنها تتميز بكونها أكثر أمانًا وأقل عرضة لإثارة استجابة مناعية.
2.3 أنواع العلاج الجيني:
- العلاج الجيني الجسدي (Somatic Gene Therapy): يستهدف الخلايا الجسدية للمريض (مثل خلايا الدم أو خلايا الكبد). لا تنتقل التغييرات الجينية التي يتم إجراؤها في هذا النوع من العلاج إلى الأجيال القادمة.
- العلاج الجيني الإنتاشي (Germline Gene Therapy): يستهدف الخلايا التناسلية للمريض (مثل الحيوانات المنوية أو البويضات). تؤدي التغييرات الجينية التي يتم إجراؤها في هذا النوع من العلاج إلى انتقالها إلى الأجيال القادمة. يثير هذا النوع من العلاج الجيني جدلاً أخلاقيًا كبيرًا بسبب آثاره المحتملة على النسل المستقبلي.
2.4 تطبيقات واعدة للعلاج الجيني:
حقق العلاج الجيني نجاحات ملحوظة في علاج بعض الأمراض الوراثية النادرة، مثل:
- ضمور الشبكية الوراثي: تمت الموافقة على أول علاج جيني لمرض وراثي في الولايات المتحدة في عام 2017 لعلاج نوع نادر من ضمور الشبكية.
- نقص المناعة المشترك الشديد (SCID): حقق العلاج الجيني نتائج واعدة في علاج هذا المرض الذي يمنع الأطفال من تطوير جهاز مناعي فعال.
- فقر الدم المنجلي والثلاسيميا: تجرى حاليًا تجارب سريرية واعدة تستخدم العلاج الجيني لتعديل الجين المسؤول عن هذه الأمراض.
- بعض أنواع السرطان: يتم تطوير علاجات جينية تستخدم الفيروسات المعدلة لقتل الخلايا السرطانية أو لتحفيز الجهاز المناعي لمهاجمة السرطان.
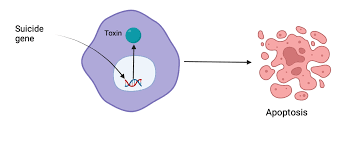
3. تحرير الجينات: جراحة جينية دقيقة
يمثل تحرير الجينات جيلاً جديدًا من التقنيات التي تسمح بإجراء تغييرات دقيقة وموجهة في تسلسل الحمض النووي داخل الخلايا الحية. على عكس العلاج الجيني التقليدي الذي غالبًا ما يضيف جينًا جديدًا دون استبدال الجين المعيب، يتيح تحرير الجينات إمكانية تصحيح الطفرات الجينية بدقة عالية.
3.1 تقنيات تحرير الجينات:
ظهرت عدة تقنيات لتحرير الجينات، ولكن أبرزها وأكثرها استخدامًا هي تقنية كريسبر-كاس9 (CRISPR-Cas9).
- كريسبر-كاس9: يعتمد هذا النظام على بروتين يسمى Cas9 يعمل كـ “مقص جزيئي” يمكنه قطع الحمض النووي في موقع محدد بدقة. يتم توجيه بروتين Cas9 إلى الموقع المستهدف في الجينوم باستخدام جزيء صغير من الحمض النووي الريبوزي (RNA) يسمى “المرشد” (guide RNA). بمجرد قطع الحمض النووي، تقوم آليات الإصلاح الطبيعية في الخلية بإصلاح الكسر. يمكن للعلماء استغلال هذه الآليات لإدخال تغييرات محددة في تسلسل الحمض النووي، مثل حذف جزء من الجين، أو إدخال جين جديد، أو تصحيح طفرة معينة.
هناك تقنيات أخرى لتحرير الجينات، مثل:
- نيوكليازات إصبع الزنك (Zinc-Finger Nucleases – ZFNs)
- نيوكليازات فعالة شبيهة بالمنشطات النسخية (Transcription Activator-Like Effector Nucleases – TALENs)
على الرغم من أن هذه التقنيات أقدم من كريسبر-كاس9، إلا أنها أقل استخدامًا بسبب تعقيد تصميمها وتكلفتها.
3.2 مزايا تحرير الجينات:
- الدقة العالية: تتيح تقنيات تحرير الجينات إجراء تغييرات دقيقة وموجهة في الجينوم، مما يقلل من احتمالية حدوث تأثيرات غير مرغوب فيها.
- الكفاءة: يعتبر نظام كريسبر-كاس9 فعالًا نسبيًا وسهل الاستخدام والتطبيق في المختبرات.
- التنوع في التطبيقات: يمكن استخدام تحرير الجينات لمجموعة واسعة من التطبيقات، بدءًا من تصحيح الأمراض الوراثية وصولًا إلى تطوير علاجات جديدة للسرطان والأمراض المعدية.
3.3 تطبيقات واعدة لتحرير الجينات:
يمتلك تحرير الجينات إمكانات هائلة في مختلف المجالات، بما في ذلك:
- علاج الأمراض الوراثية: يمكن استخدام تحرير الجينات لتصحيح الطفرات الجينية المسببة للأمراض مثل التليف الكيسي، وفقر الدم المنجلي، ومرض هنتنغتون. تجرى حاليًا تجارب سريرية واعدة في هذا المجال.
- تطوير نماذج حيوانية للأمراض: يمكن استخدام تحرير الجينات لإنشاء حيوانات تحمل طفرات جينية محددة، مما يساعد الباحثين على فهم آليات المرض وتطوير علاجات جديدة.
- الهندسة الوراثية للمحاصيل والحيوانات: يمكن استخدام تحرير الجينات لتحسين صفات المحاصيل الزراعية والحيوانات، مثل زيادة الإنتاجية ومقاومة الأمراض.
- علاج السرطان: يمكن استخدام تحرير الجينات لتعديل الخلايا المناعية للمريض لجعلها أكثر قدرة على التعرف على الخلايا السرطانية وقتلها.
- مكافحة الأمراض المعدية: يمكن استخدام تحرير الجينات لتطوير علاجات جديدة للأمراض الفيروسية والبكتيرية.
4. الاعتبارات الأخلاقية والمجتمعية والقانونية
على الرغم من الإمكانات الهائلة للعلاج الجيني وتحرير الجينات، إلا أنهما يثيران العديد من الاعتبارات الأخلاقية والمجتمعية والقانونية التي يجب معالجتها بعناية.
4.1 المخاوف المتعلقة بالسلامة:
- التأثيرات غير المستهدفة: قد تؤدي تقنيات تحرير الجينات إلى إجراء تغييرات غير مقصودة في مواقع أخرى من الجينوم، مما قد يكون له آثار ضارة.
- الاستجابة المناعية: قد يثير إدخال مواد وراثية غريبة إلى الجسم استجابة مناعية غير مرغوب فيها.
- الآثار طويلة المدى: لا يزال من غير الواضح تمامًا ما هي الآثار طويلة المدى للعلاج الجيني وتحرير الجينات على صحة الإنسان.
4.2 المعضلات الأخلاقية:
- تحرير الخلايا الإنتاشية (Germline Editing): يثير تحرير الجينات في الخلايا التناسلية مخاوف أخلاقية كبيرة بسبب إمكانية نقل التغييرات الجينية إلى الأجيال القادمة. هناك قلق من أن هذا قد يؤدي إلى عواقب غير متوقعة على التطور البشري.
- “أطفال المصممين” (Designer Babies): هناك قلق من أن استخدام تحرير الجينات لأغراض غير علاجية، مثل تحسين الصفات الجسدية أو العقلية، قد يؤدي إلى تفاقم عدم المساواة الاجتماعية.
- الموافقة المستنيرة: يجب التأكد من أن المرضى المشاركين في التجارب السريرية للعلاج الجيني وتحرير الجينات يفهمون تمامًا المخاطر والفوائد المحتملة قبل إعطاء موافقتهم.
4.3 القضايا المجتمعية والقانونية:
- الوصول إلى العلاجات: يجب ضمان أن تكون هذه العلاجات المبتكرة متاحة لجميع المرضى الذين يحتاجون إليها، بغض النظر عن وضعهم الاجتماعي والاقتصادي.
- التنظيم القانوني: هناك حاجة إلى وضع أطر قانونية وتنظيمية واضحة لتوجيه تطوير واستخدام العلاج الجيني وتحرير الجينات بشكل مسؤول وآمن.
- النقاش العام: من الضروري إجراء نقاش عام مستنير حول الآثار الأخلاقية والمجتمعية للعلاج الجيني وتحرير الجينات لضمان أخذ وجهات نظر مختلفة في الاعتبار.

5. آفاق المستقبل والتحديات المستمرة
يمثل العلاج الجيني وتحرير الجينات مجالات بحثية سريعة التطور. تشير التطورات الأخيرة إلى مستقبل واعد لعلاج مجموعة واسعة من الأمراض. ومع ذلك، لا تزال هناك العديد من التحديات التي يجب التغلب عليها لكي تصبح هذه التقنيات علاجات روتينية وآمنة وفعالة.
5.1 التحديات الحالية:
- تحسين طرق التوصيل: لا تزال طرق توصيل الجينات إلى الخلايا المستهدفة غير فعالة في بعض الأحيان. هناك حاجة إلى تطوير نواقل أكثر أمانًا وكفاءة.
- تقليل التأثيرات غير المستهدفة: يجب تحسين دقة تقنيات تحرير الجينات لتقليل احتمالية حدوث تغييرات غير مقصودة في الجينوم.
- فهم الآثار طويلة المدى: هناك حاجة إلى إجراء المزيد من البحوث لفهم الآثار طويلة المدى للعلاج الجيني وتحرير الجينات على صحة الإنسان.
- خفض التكاليف: غالبًا ما تكون علاجات الجينات باهظة الثمن، مما يجعلها غير متاحة للكثير من المرضى. هناك حاجة إلى تطوير طرق لخفض تكاليف هذه العلاجات.
5.2 الاتجاهات المستقبلية:
- العلاج الجيني الشخصي: من المتوقع أن يلعب العلاج الجيني دورًا متزايد الأهمية في الطب الشخصي، حيث يتم تصميم العلاجات خصيصًا لتناسب التركيب الجيني الفريد لكل مريض.
- تطوير علاجات جديدة للسرطان: من المتوقع أن يشهد مجال علاج السرطان ثورة بفضل العلاجات الجينية وتقنيات تحرير الجينات التي تستهدف الخلايا السرطانية بشكل مباشر أو تعزز استجابة الجهاز المناعي.
- الوقاية من الأمراض: في المستقبل، قد يكون من الممكن استخدام العلاج الجيني للوقاية من بعض الأمراض الوراثية أو حتى الأمراض المعدية.
- تطوير تقنيات تحرير جينات أكثر دقة: يستمر الباحثون في تطوير تقنيات جديدة لتحرير الجينات تكون أكثر دقة وأمانًا وكفاءة.
الخلاصة
يمثل العلاج الجيني وتحرير الجينات قفزة نوعية في مجال الطب، حيث يوفران إمكانية علاج الأمراض التي كانت تعتبر في السابق غير قابلة للشفاء. على الرغم من التحديات الأخلاقية والمجتمعية والقانونية التي تصاحب هذه التقنيات، فإن الإمكانات الهائلة التي تحملها في طياتها تجعلها من أهم المجالات البحثية في عصرنا الحالي. مع استمرار التقدم العلمي والتنظيم المسؤول، يمكن للعلاج الجيني وتحرير الجينات أن يحدثا ثورة حقيقية في عالم الطب ويحسنا حياة الملايين من الناس حول العالم. من الضروري مواصلة البحث والتطوير في هذا المجال مع الأخذ في الاعتبار الجوانب الأخلاقية والمجتمعية لضمان استخدام هذه التقنيات بشكل يخدم البشرية جمعاء.